|
熵与能量一样,是一个真实的物理量,它使不同形式的转变可以相互比较。
1. 熵的热力学意义
热量Q从高温热源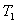 传递到低温热源 传递到低温热源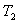 ,高温热源的熵变为 ,高温热源的熵变为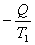 (这里设 (这里设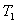 不变,类似设 不变,类似设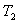 不变),低温热源的熵变为 不变),低温热源的熵变为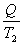 ,其中负号表示放出热量,则系统的熵变为 ,其中负号表示放出热量,则系统的熵变为
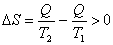
 系统的熵增加了,其意义是什么呢? 系统的熵增加了,其意义是什么呢?
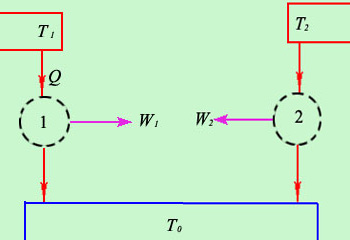
我们从做功的角度来考虑,设另有一低温热源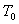 ,满足 ,满足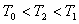 。分别从高温热源
。分别从高温热源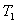 、 、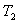 取出热量Q(如右图所示),利用效率最大的卡诺循环将其尽可能多地转变为功,则有
取出热量Q(如右图所示),利用效率最大的卡诺循环将其尽可能多地转变为功,则有
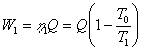
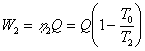
两次做功的差别为
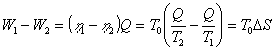
可见,对于同样热量Q,转变为功的可能性是不一样的,有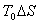 的热量不能转变为功,这部分热量正比于
的热量不能转变为功,这部分热量正比于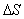 ,所以,我们说熵的增加表示系统热量转变为功的可能性减少,即系统能量的品质变坏了。 ,所以,我们说熵的增加表示系统热量转变为功的可能性减少,即系统能量的品质变坏了。
2. 熵的统计物理意义
熵作为一个热力学量,它的微观意义是什么呢?
玻尔兹曼从分子运动论的角度考察了熵。在系统总能量、总分子数一定的情况下,证明了表征系统宏观状态的熵与该宏观状态对应的微观态数W有如下关系
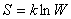 , ,
这就是著名的玻尔兹曼公式,它把熵与系统微观状态数联系起来,系统的熵越大,其微观状态数越多,分子运动越混乱。它揭示了熵的统计意义:熵是系统微观状态数或热力学概率的量度。
普朗克从熵的基本性质出发,也分析得到了玻尔兹曼公式。
假定熵S与热力学概率W之间的关系用一般函数关系表示为
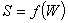
由于S广延量,系统总熵等于系统两部分的熵之和,即有
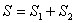
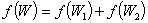
根据几率的运算法则,系统两部分中特定状态同时出现的几率是这两部分特定状态各具有的几率的乘积,即有
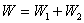
要使上述两种运算关系都能满足,f(W)应该是对数函数,即
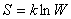
|