

|
||
 1842年确立了能量守恒与转换定律,人们认识到热不是流体,不存在“热质”或者“热素”等东西,热是组成物体的大量的粒子无规则运动的宏观表现,热只是能量存在的一种形式;热和功可以相互转化。 这就向人们提出一个问题,能量守恒与转换定律和卡诺定理之间是否存在矛盾:能量守恒与转换指出,能量既不会创生,也不会消灭,只能从一种形式转化为另一种形式。也就是说,功可以转变成热,热也可以转变成功,这不违背能量守恒定律。卡诺定理却向人们表明:热不能全部转变成为功,当热量 克劳修斯还发现,负转变就是正转变的逆过程,正转变可以自发进行,而负转变不能自发进行,即正转变是一种不可逆的变化。 克劳修斯为了研究正、负转变的数量,度量不可逆性,花了15年的时间进行研究。19世纪中叶,由于引入了“热功当量”,使热力学第一定律(即包括热现象在内的能量守恒定律)有了数学解析表达式。这给克劳修斯一个有益的启示,应该寻找一个“转变含量”或者“变换容度”,把不同形式的转变相互比较,从而使热力学第二定律定量化。 克劳修斯从热变换理论着手,在计算变换的“等价量”中提出了熵,熵的变化规律表征了不可逆过程的共同特征。克劳修斯进一步发挥了卡诺的思想,设计了一个包括四个膨胀阶段和两个压缩阶段,一共六个阶段的可逆循环过程(如下图所示,称为克劳修斯循环)。通过对克劳修斯循环的研究,得出了著名的克劳修斯等式和克劳修斯不等式
克劳修斯定义
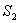 与它的始态值 与它的始态值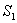 之差,即 之差,即
这个S就是克劳修斯的变换容度。他建议称S为熵Entropy。它源于“变换”的希腊词“trope”,加上前缀En,以便与能量(energy)这个词对应。在克劳修斯看来,熵和能这两个概念是有某种相似性的,能从正面量度运动转化的能力,能越大,运动转化的能力越大。熵却从反面,即运动不能转化的一面量度运动转化的能力,表示着转化已经完成的程度,即运动丧失转化能力的程度。 |