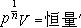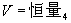如图(3)所示,一绝热容器分成相等的两部分,左半部充以理想气体,右半部为真空。开始时理想气体处于平衡状态。打开管闩后,气体冲入右半部,最后达到新的平衡态。这一过程称为气体向真空的绝热自由膨胀过程。
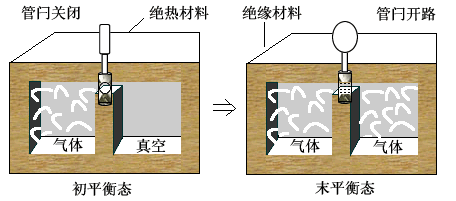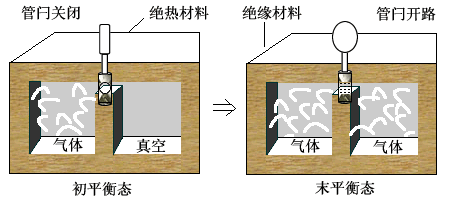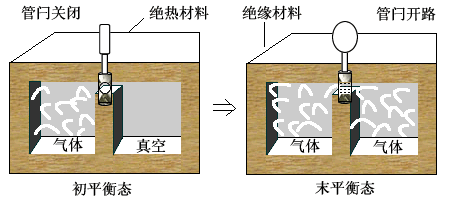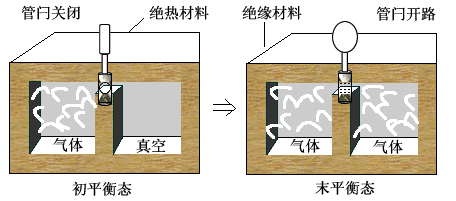
图(3) 自由膨胀。由于没有热量 Q 传递与外界做功 A',所以内能
E 保持不变
由热力学第一定律: Q = 0 ,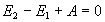
由于气体是向真空膨胀,对外不做功,即 A = 0,所以
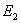 - -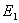 =0 =0
由于理想气体内能只包含分子热运动动能,内能不变意味着膨胀前后初态与末态温度相等,即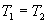 (为什么?);由初态、末态理想气体状态方程可得: (为什么?);由初态、末态理想气体状态方程可得:
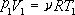
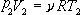
将 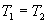 , , 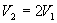 代入上两式,则得膨胀后的压强为
代入上两式,则得膨胀后的压强为
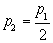
即膨胀前后温度不变,体积增大一倍,压强减小1/2。
说明:
1.对于实际气体(真实气体)经绝热膨胀后,温度一般不会恢复到原来温度,请读者思考这是为什么?
2.理想气体向真空膨胀的过程是一个理想过程,实际应用中可利用实际气体向压强较低的区域膨胀,例如将实际气体通过多孔塞流入相对压强较小的区域来改变气体的温度。
气体实际进行的过程既非等温过程,也非绝热过程,往往可以用多方过程表示,简要说明如下:
1.多方过程方程

式中 n 为任意常数,称为多方指数。凡满足上述方程的过程称为多方过程。在热力工程、化学工业等工程技术中有广泛应用。
①当 n =1
时, 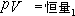 ──等温过程方程 ──等温过程方程
②当 n = 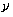 时,
时, 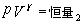 ──绝热过程方程 ( ──绝热过程方程 (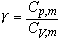 ) )
③当 n =0
时, 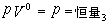 ──等压过程方程 ──等压过程方程
④当 n = ∞
时, 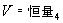 ──等体过程方程
──等体过程方程
⑤当1<n < 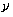 时,且满足
时,且满足 ──介于等温、绝热过程之间的过程 ──介于等温、绝热过程之间的过程
|
 ,即
,即