玻意耳(Robert
Boyle,1627-1691 ),英国物理学家。
盖.吕萨克(Joseph
Lussac,1778-1850),法国化学家
玻耳兹曼(Ludwig
Boltzmann,1884-1906),奥地利物理学家。
根据阿伏加德罗定律:在同温同压下,同体积的任何气体含有相同数目的分子,由此可知,分子数目相同的任何气体在同温同压下都占有相同的体积,在标准状态下,1mol的任何气体都占有22.4
l(升)的体积。
摩尔是表示物质的量的基本单位,国际上规定:任何物质之中含有
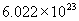
个微粒(如分子、原子、离子、电子……等)的这一物质量,称为1摩尔,简称摩,符号为mol
严导淦编《物理学》第3版上册,p465~471北京,高教出版社
程守洙、江之永编《普通物理学》第5版第一册,p268~270,北京,高教出版社
马文尉编《物理学》第4版上册,p179~180,北京,高教出版社
马文尉编《习题分析与解答》,北京,高教出版社
张三慧编《大学物理学》第2版第2册:热学,p1~14,北京,清华大学出版社
吴百诗编《大学物理学》修订版下册,p6~8,西安交通大学出版社
吴锡珑编《大学物理教程》第一册,p301~305,上海交通大学出版社 |
查理
(Jacquse Alexandre-Cesar Charles,1746-1823),法国物理学家
|
|
03-08-02
气体的实验定律
理想气体的状态方程

本节从气体三条实验定律出发,推导理想气体状态方程的三种形式。
|
|
|
|
|
|
|
|
玻意耳定律 一定质量的气体,当温度保持不变时,它的压强与体积的乘积等于恒量。即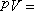 恒量,亦即在一定温度下,对一定量的气体,它的体积与压强成反比。 恒量,亦即在一定温度下,对一定量的气体,它的体积与压强成反比。
盖.吕萨克定律 一定质量的气体,当压强保持不变时,它的体积与热力学温度成正比。即 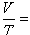 恒量 恒量
查理定律 一定质量的气体,当体积保持不变时,它的压强与热力学温度成正比,即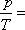 恒量。 恒量。
气体实验定律的适用范围:只有当气体的温度不太低(与室温相比),压强不太大(与大气压相比)时,方能遵守上述三条定律。
如果气体在压强很大,温度又很低,即气体很不稀薄甚至接近液化时,实验结果与上述定律相比会有很大的偏差。
在任何情况下都遵守玻意耳、盖.吕萨克及查理定律的气体,称为理想气体。
一般真实气体,如氮、氧、氢、氦等,在温度不太低,压强不太大时,都可以近似看做理想气体。理想气体是真实气体的一个理想模型。

设某一容器内有一定的质量为M ,摩尔质量为μ的理想气体,初始的平衡状态为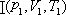 ,在状态发生改变后,过渡到新的平衡态 ,在状态发生改变后,过渡到新的平衡态
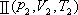 ,其中间可以经过各种不同的过程。由气体的实验定律可以推导出气体在初、末两个平衡态的六个状态参量的关系为 ,其中间可以经过各种不同的过程。由气体的实验定律可以推导出气体在初、末两个平衡态的六个状态参量的关系为
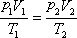 (1)
(1) |
|
|
|
|
|
|
上式(1)即为理想气体状态方程的初步形式。关系式(1)不仅适用于 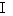 、 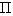
两个平衡态,还可推广到其他任何平衡态,即
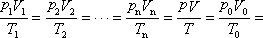 恒量
其中 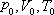
为标准状态下气体的状态参量。由 阿伏伽德罗定律,在 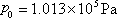 ,
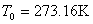 时, 1mol任何气体的体积都为 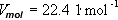
,则 摩尔数为 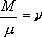
的理想气体在标准状态下的体积为 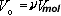
,代入上式,可得 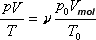
我们引进一个对任何气体都普遍适用的常量 R,称为普适气体常量:
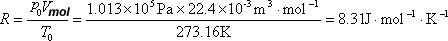 则上式可写成简单的形式:
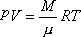
(2)
(2)
上式表示了理想气体在任一平衡态下各宏观状态参量 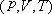 之间的关系,称为理想气体状态方程。 之间的关系,称为理想气体状态方程。
理想气体状态方程还可以化为另一种常用的形式,即
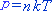 (3)
(3)
其中n为单位气体体积内分子的个数,称为气体分子数密度;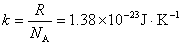 称为玻耳兹曼常量,而 称为玻耳兹曼常量,而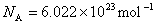 称为阿伏加德罗常量。 称为阿伏加德罗常量。
|
|
|
|
|
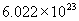 个微粒(如分子、原子、离子、电子……等)的这一物质量,称为1摩尔,简称摩,符号为mol
个微粒(如分子、原子、离子、电子……等)的这一物质量,称为1摩尔,简称摩,符号为mol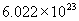 个微粒(如分子、原子、离子、电子……等)的这一物质量,称为1摩尔,简称摩,符号为mol
个微粒(如分子、原子、离子、电子……等)的这一物质量,称为1摩尔,简称摩,符号为mol