分子平均动能>>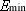 时,物质处于气态
时,物质处于气态
分子平均动能<<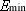 时,物质处于固态
时,物质处于固态
分子平均动能 ≈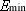 时,物质处于液态
时,物质处于液态
分子平均动能>>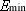 时,物质处于气态
时,物质处于气态
分子平均动能<<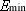 时,物质处于固态
时,物质处于固态
分子平均动能 ≈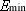 时,物质处于液态
时,物质处于液态
| 严导淦编《物理学》,第3版上册,北京,高教出版社 程守洙、江之永编《普通物理学》,第5版,第一册,北京,高教出版社 马文尉编《物理学》,第4版,上册,北京,高教出版社 马文尉编《习题分析与解答》,北京,高教出版社 张三慧编《大学物理学》,第2版,第2册:热学,北京,清华大学出版社 吴百诗编《大学物理学》,修订版,下册,西安交通大学出版社 |

|
|||||||||||
| 首页 | 后退 |
|
||||||||||
03-08-03
气体动理论的基本观点
|
|
|||||||||||||||||||||||