|
бЯЕМфЦБрЁЖЮяРэбЇЁЗЃЌЕк3АцЩЯВсЃЌББОЉЃЌИпНЬГіАцЩчЃЌ1998
еХШ§ЛлБрЁЖДѓбЇЮяРэбЇЁЗЃЌЕк2АцЃЌЕк2Вс:ШШбЇЃЌББОЉЃЌЧхЛЊДѓбЇГіАцЩчЃЌ2000ЃЌ1
ЮтАйЪЋБрЁЖДѓбЇЮяРэбЇЁЗЃЌаоЖЉАцЃЌЯТВсЃЌББОЉЃЌЮїАВНЛЭЈДѓбЇГіАцЩчЃЌ1995ЃЌ12
ТэЮФЮОБрЁЖЮяРэбЇЁЗЃЌЕк5АцЃЌЕквЛВсЃЌББОЉЃЌИпНЬГіАцЩчЃЌ1998ЃЌ6
КњХЬаТИФБр(ГЬЪифЈЁЂНжЎгРжїБр)ЁЖЦеЭЈЮяРэбЇЁЗЃЌЕк5АцЃЌББОЉЃЌИпНЬГіАцЩч
ЮтЮ§ччжїБрЁЖДѓбЇЮяРэбЇЁЗЩЯКЃНЛЭЈДѓбЇГіАцЩч
едПЛЊЁЂТоЮЕв№БржјЁЖаТИХФюЮяРэНЬГЬЁЗЕк2ОэЃЌББОЉЃЌИпНЬГіАцЩч |

ЁЁЁЁзДЬЌЫцЪБМфЕФБфЛЏГЦЮЊЁАЙ§ГЬЁБЁЃШШСІбЇЯЕЭГЕФзДЬЌЫцЪБМфБфЛЏЕФЙ§ГЬГЦЮЊШШСІбЇЙ§ГЬЁЃгЩгкжаМфзДЬЌВЛЭЌЃЌШШСІбЇЙ§ГЬПЩЗжЮЊСНжжРраЭЃК
ЁЁЁЁ1ЃЎЗЧОВЬЌЙ§ГЬЃЈгжГЦЗЧЦНКтЙ§ГЬЃЉ
ЁЁЁЁФГШШСІбЇЯЕЭГДгЪМЬЌЃЈЦНКтЬЌЃЉОвЛЯЕСаБфЛЏЕНДяжеЬЌЃЈЦНКтЬЌЃЉЃЌОРњСЫДгЦНКтЬЌЕНЗЧЦНКтЬЌЃЈЯЕЭГИїВПЗжзДЬЌВЮСПВЛОљдШЃЉЁЂдйЕНЦНКтЬЌЕФЙ§ЖЩЁЃетжжЪМФЉСНЬЌжЎМфЫљОРњЕФжаМфзДЬЌЮЊЗЧЦНКтЬЌЕФЙ§ГЬГЦЮЊЗЧОВЬЌЙ§ГЬЁЃР§ШчЭЦЖЏЛюШћПьЫйбЙЫѕЦјИзФкЕФЦјЬхЁЃ
ЁЁЁЁ2ЃЎзМОВЬЌЙ§ГЬ
ЁЁЁЁЂй ЖЈвхЃКЯЕЭГдкЪМФЉСНЦНКтЬЌжЎМфШЮвтЪБПЬЫљОРњЕФжаМфзДЬЌЖМПЩНќЫЦЕиЪгЮЊЦНКтЬЌЕФЙ§ГЬЃЌГЦЮЊзМОВЬЌЙ§ГЬЃЌЛђепЫЕЁАзМОВЬЌЙ§ГЬЪЧгЩвЛЯЕСавРДЮНгЬцЕФЦНКтЬЌЫљзщГЩЕФЙ§ГЬЁБЁЃ
ЁЁЁЁЯЕЭГЪмЭтНчзїгУДгвЛИіЦНКтЬЌзмвЊДђЦЦЦНКтВХФмДяЕНСэвЛИіЦНКтЬЌЃЌФЧУДЁАзМОВЬЌЙ§ГЬЁБШчКЮЪЕЯжФиЃП
ЁЁЁЁЂк ЪЕЯжЁАзМОВЬЌЙ§ГЬЁБЕФЬѕМўЃКзМОВЬЌЙ§ГЬЪЧвЛжжРэЯыЙ§ГЬЃЌЕБЪЕМЪЙ§ГЬНјааЕУЮоЯоЛКТ§ЪБЃЌИїЪБПЬЯЕЭГЕФзДЬЌОЭЮоЯоЕиНгНќгкЦНКтЬЌЃЌИУЙ§ГЬБуЪЧзМОВЬЌЙ§ГЬЁЃШчЭМЫљЪО
| ЁЁЁЁЂлзМОВЬЌЙ§ГЬПЩгУЯЕЭГЕФзДЬЌЭМЃЈШчp
- V ЭМЛђp - T ЭМЛђV
-T ЭМЃЉжаЕФвЛЬѕЧњЯпБэЪОЁЃЧыПДгвЭМЁЃзДЬЌЭМЩЯШЮКЮвЛЕуБэЪОЯЕЭГЕФвЛИіЦНКтЬЌЁЃгЩвЛЯЕСаЦНКтЬЌзщГЩЕФзМОВЬЌЙ§ГЬдкp
- V зДЬЌЭМжагУвЛЬѕСЌајЧњЯпРДБэЪОЁЃ |
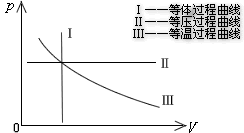 Ѓ Ѓ p-V
Ѓ Ѓ p-VЭМЩЯМИЬѕзМОВЬЌЙ§ГЬЧњЯп |
|
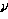 =
=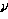 =
=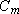 жЕНдгыЙ§ГЬгаЙиЁЃ
жЕНдгыЙ§ГЬгаЙиЁЃ