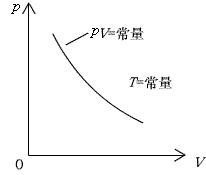
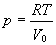|
ЁЁЁЁ
Ѓ Ѓ ЫМПМЬт:МИжжЮяжЪЕФСйНчВЮСПШчЯТБэЫљЪОЁЃФуФмДгБэжаЫљИјЪ§ОнЗжЮіГіФФаЉЦјЬхНЯШнвзБЛвКЛЏЃЌФФаЉЦјЬхзюФбБЛвКЛЏТ№ЃП
Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ МИжжЦјЬхЕФСйНчВЮСП
ЁЁЁЁ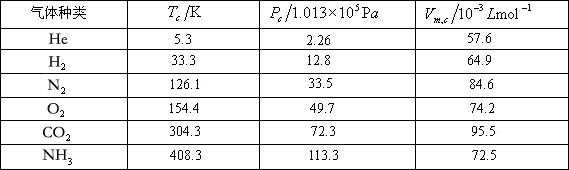
ЁЁЁЁЬсЪО:ЧызЂвтИїжжЦјЬхСйНчЮТЖШ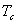 ЕФИпЕЭВювьЃЌЯывЛЯыСйНчЮТЖШНЯИпЕФЦјЬхЕШЮТбЙЫѕвзгквКЛЏТ№ЃПЛЙЪЧЯрЗДЃП
ЕФИпЕЭВювьЃЌЯывЛЯыСйНчЮТЖШНЯИпЕФЦјЬхЕШЮТбЙЫѕвзгквКЛЏТ№ЃПЛЙЪЧЯрЗДЃП
ЁЁЁЁКЩРМЮяРэбЇМвЗЖЕТЭпЖњЫЙдЫгУЦјЬхЗжзгЖЏРэТлЕФдРэЃЌПМТЧСЫецЪЕЦјЬхЗжзгЬхЛ§КЭЗжзгМфв§СІЕФгАЯьЁЃВЩгУгав§СІИжадЧђЗжзгФЃаЭЃЌЖдРэЯыЦјЬхзДЬЌЗНГЬМгвдаое§ЃЌДгЖјНЈСЂСЫецЪЕЦјЬхЕФзДЬЌЗНГЬЁЃ
ЁЁЁЁ1ЃЎецЪЕЦјЬхЗжзгФЃаЭЉЄЉЄгаЮќв§СІЕФИжадЧђФЃаЭ
ЁЁЁЁЪЕбщКЭРэТлЗжЮіБэУїЃЌЗжзгМфДцдкЯрЛЅзїгУСІЃЌСНЗжзгМфзїгУСІЫцСНЗжзгжааФжЎМфЕФОрРыrЕФБфЛЏЧщПіЃЌШчЭМЫљЪОЁЃ гЩЭМПЩПДГі:ЕБСНЗжзгНгНќЕН 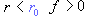 ЃЌМДЗжзгМфЯрЛЅзїгУСІбИЫйдіДѓЃЌзшжЙСНепНјвЛВНППНќЃЌСНЗжзгжааФЯрОрd ЪБЃЌГтСІfЁњЁоЃЌгкЪЧЃЌЮвУЧБуАбЗжзгПДзїжБЯпЮЊd( ЃЌМДЗжзгМфЯрЛЅзїгУСІбИЫйдіДѓЃЌзшжЙСНепНјвЛВНППНќЃЌСНЗжзгжааФЯрОрd ЪБЃЌГтСІfЁњЁоЃЌгкЪЧЃЌЮвУЧБуАбЗжзгПДзїжБЯпЮЊd(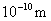 СПМЖ)ЕФЧђЬхЁЃ СПМЖ)ЕФЧђЬхЁЃ
ЁЁЁЁ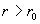 ЃЌв§СІЦ№жївЊзїгУЃЌв§СІгааЇзїгУОрРыs
дМЮЊdЕФМИЪЎБЖЕНМИАйБЖЁЃ ЃЌв§СІЦ№жївЊзїгУЃЌв§СІгааЇзїгУОрРыs
дМЮЊdЕФМИЪЎБЖЕНМИАйБЖЁЃ
ЁЁЁЁИљОнЗжзгМфЯрЛЅзїгУЕФЬиеїЃЌШЫУЧНЈСЂСЫБШРэЯыЦјЬхЗжзгФЃаЭИќНгНќЪЕМЪЕФЦјЬхЗжзгФЃаЭИжадЧђФЃаЭЁЃ
ЁЁЁЁ2ЃЎецЪЕЦјЬхзДЬЌЗНГЬ
ЁЁЁЁИљОнИжадЧђЗжзгФЃаЭЃЌЖд1molРэЯыЦјЬхзДЬЌЗНГЬМгвдаое§ЃЌНЈСЂаТЕФЗНГЬЁЃ
ЁЁЁЁЬхЛ§аое§
ЁЁЁЁАбЗжзгПДГЩЪЧИеадЧђЃЌвђОпгаЙЬгаЬхЛ§ЖјЪЙ1molЦјЬхПЩБЛбЙЫѕЕФПеМфЬхЛ§МѕЩйЮЊ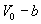 ЃЌbЮЊЗДгГЗжзгЙЬгаЬхЛ§ЕФаое§СПЁЃЫљвдЃЌРэЯыЦјЬхзДЬЌЗНГЬгІаое§ЮЊ ЃЌbЮЊЗДгГЗжзгЙЬгаЬхЛ§ЕФаое§СПЁЃЫљвдЃЌРэЯыЦјЬхзДЬЌЗНГЬгІаое§ЮЊ
ЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁ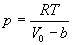 ЁЁЁЁЁЁЁЁЃ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ ЁЁ(1) ЁЁЁЁЁЁЁЁЃ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ ЁЁ(1)
ЁЁЁЁбЙЧПаое§
ЁЁЁЁПМТЧЕНЗжзгМфЕФв§СІзїгУЪБЃЌЗжзгЖдЦїБкЕФХізВЛсЪмЕНЪВУДгАЯьЃП
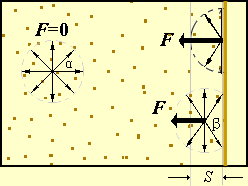
ЁЁЁЁШчЭМЫљЪОЃЌДІгкШнЦїЕБжаЕФЗжзгІСЃЌЗВжааФЮЛгквдІСЮЊЧђаФЃЌв§СІгааЇзїгУОрРыS
ЮЊАыОЖЕФЧђФкЕФЗжзгЃЌгЩгкЗжзгЖдГЦЗжВМЃЌЫќУЧЖдІСЕФв§СІзїгУЯрЛЅЕжЯћЁЃІСЗжзгКУЯёВЛЪмв§СІзїгУЃЛДІгкОрЦїБкКёЖШЮЊs
ЕФБэУцВуФкЕФЗжзгІТЃЌгЩгкЖдЫќгав§СІзїгУЕФЗжзгЗжВМВЛОљдШЃЌЪЙІТЗжзгЦНОљЪмЕНвЛИіжИЯђЦјЬхФкВПЕФКЯСІFЃЌДгЖјМѕЩйЗжзгзїгУгкШнЦїБкЕФГхСПЃЌЪЙЫќЖдЦїБкзїгУЕФбЙЧПМѕЩйЮЊ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ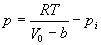 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ(2) ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ(2)
ЪНжаpЮЊЦјЬхЗжзгЪЕМЪзїгУгкЦїБкЕФбЙЧПЃЌМДЮЊЪЕбщПЩВтГіЕФбЙЧПЁЃ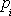 ЮЊЗжзгФкбЙЧПЃЌ
ЮЊЗжзгФкбЙЧПЃЌ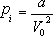 ЃЌaЮЊЗДгГЗжзгМфв§СІзїгУЕФаое§СПЃЌaЁЂbЪ§жЕПЩгЩЪЕбщВтЖЈЁЃНЋ ЃЌaЮЊЗДгГЗжзгМфв§СІзїгУЕФаое§СПЃЌaЁЂbЪ§жЕПЩгЩЪЕбщВтЖЈЁЃНЋ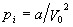 ДњШы(2)ЪНЃЌдђЪБЃЌ1molЦјЬхЕФзДЬЌЗНГЬЮЊ ДњШы(2)ЪНЃЌдђЪБЃЌ1molЦјЬхЕФзДЬЌЗНГЬЮЊ
ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ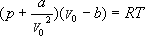 ЁЁЁЁЁЁЁЁЁЁ(3) ЁЁЁЁЁЁЁЁЁЁ(3)
ЖдгкжЪСПЮЊMЃЌФІЖћжЪСПЮЊ ІЬ ЕФецЪЕЦјЬхЕФзДЬЌЗНГЬгІЮЊ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ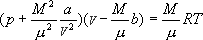 ЁЁЁЁЁЁ(4)
ЁЁЁЁЁЁ(4)
ЁЁЁЁЩЯЪНГЦЮЊЗЖЕТЭпЖњЫЙЗНГЬЁЃЫќВЛНіЖдецЪЕЦјЬхЦЋРыРэЯыЦјЬхЕФаджЪзїСЫЖЈадНтЪЭЃЌжИГіЦјЬхДцдкСйНчЕуЃЌЖдвКЬЌКЭЦјЬЌЯрБфИјГіСЫФГжжНтЪЭЃЌОпгавЛЖЈЕФРэТлКЭЪЕМЪвтвхЁЃ
ЁЁЁЁЯТБэИјГідкЮТЖШ 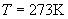 ЯТЃЌ1molЕФN2ЃЌЦфбЙЧПгЩ1atm(Ёж ЯТЃЌ1molЕФN2ЃЌЦфбЙЧПгЩ1atm(Ёж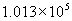
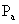 )діДѓЕН1000atm(Ёж )діДѓЕН1000atm(Ёж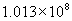
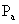 )Й§ГЬжаЃЌВтГіЕФУПвЛбЙЧПЯТN2ЕФЬхЛ§V0ЁЃНЋЫќУЧЗжБ№ДњШыРэЯыЦјЬхзДЬЌЗНГЬ( )Й§ГЬжаЃЌВтГіЕФУПвЛбЙЧПЯТN2ЕФЬхЛ§V0ЁЃНЋЫќУЧЗжБ№ДњШыРэЯыЦјЬхзДЬЌЗНГЬ(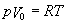 )КЭЗЖЕТЭпЖњЫЙЗНГЬЃЈЪН4ЃЉВЂНјааБШНЯЁЃ )КЭЗЖЕТЭпЖњЫЙЗНГЬЃЈЪН4ЃЉВЂНјааБШНЯЁЃ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ ЗЖЕТЭпЖњЫЙЗНГЬгыРэЯыЦјЬхЗНГЬЕФБШНЯ(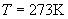 ) )
ЁЁЁЁ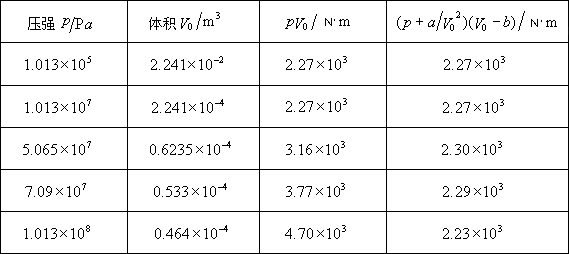
ЁЁЁЁ
ЁЁЁЁБэжаЯдЪОЃЌЕБ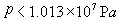 (МД100atm)ЪБЃЌСНЗНГЬЗћКЯЕФНЯКУЃЌЖМФмНЯКУЕиЗДгГN2ЕФЙцТЩЃЛЕБ (МД100atm)ЪБЃЌСНЗНГЬЗћКЯЕФНЯКУЃЌЖМФмНЯКУЕиЗДгГN2ЕФЙцТЩЃЛЕБ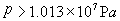 ЪБЃЌСНЗНГЬИјГіЕФМЦЫуНсЙћВюБ№дНРДдНДѓЃЌЦфжаЗЖЕТЭпЖњЫЙЗНГЬШдФмНЯКУЕиЗДгГN2ЕФааЮЊЃЌЕЋРэЯыЦјЬхзДЬЌЗНГЬвбВЛФмЗДгГN2КЭааЮЊСЫЁЃ ЪБЃЌСНЗНГЬИјГіЕФМЦЫуНсЙћВюБ№дНРДдНДѓЃЌЦфжаЗЖЕТЭпЖњЫЙЗНГЬШдФмНЯКУЕиЗДгГN2ЕФааЮЊЃЌЕЋРэЯыЦјЬхзДЬЌЗНГЬвбВЛФмЗДгГN2КЭааЮЊСЫЁЃ
ЗЖЕТЭпЖњЫЙЕШЮТЯпЃЌШчЭМЫљЪОЁЃ
ЁЁЁЁ
ЁЁЁЁЖдгкРэЯыЦјЬхЃЌгЩгкКіТдЗжзгМфЯрЛЅзїгУЪЦФмЃЌРэЯыЦјЬхФкФмжЛЪЧЮТЖШЕФКЏЪ§ЃЌМД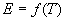 ЁЃ ЁЃ
ЁЁЁЁЖдгкецЪЕЦјЬхЃЌдђБиаыПМТЧЗжзгМфЕФЯрЛЅзїгУСІЃЌЙЪЗжзгМфгаЯрЛЅзїгУЪЦФмЁЃвђДЫЃЌЦНКтЬЌЯТецЪЕЦјЬхЕФФкФмЃЌЪЧУПИіЗжзгздЩэЕФФмСП(ЪЧЮТЖШT
ЕФКЏЪ§)гыЗжзгМфЕФЯрЛЅзїгУЪЦФм(гыЗжзгЯрЖдЮЛжУгаЙиЃЌЪЧЬхЛ§ЕФКЏЪ§)жЎзмКЭЃЌМДецЪЕЦјЬхФкФмЪЧЮТЖШКЭЬхЛ§ЕФКЏЪ§ЃЌПЩБэЪОЮЊ
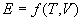
ФкФмE ЕФОпЬхаЮЪНЃЌПЩгЩЪЕбщВтЖЈЛђРэТлЕМГіЃЌЖдЗЖЕТЭпЖњЫЙЦјЬхФЃаЭЃЌРэТлЕМГіЕФФкФмаЮЪНЮЊ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ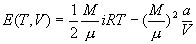 ЁЁЁЁЁЁ(5)
ЁЁЁЁЁЁ(5)
ЁЁЁЁЪНжаЁЁi -- ЦјЬхЗжзгздгЩЖШ(ГЃЮТЯТ)
ЁЁЁЁЁЁ ЁЁ a -- ЗДгГЗжзгМфв§СІзїгУЕФаое§СП
|

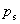 ГЦЮЊБЅКЭеєЦћбЙЁЃдквЛЖЈЕФЮТЖШЯТ
ГЦЮЊБЅКЭеєЦћбЙЁЃдквЛЖЈЕФЮТЖШЯТ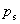 гавЛЖЈжЕЁЃР§Шч13ЁцЪБ
гавЛЖЈжЕЁЃР§Шч13ЁцЪБ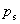 ЃН49atm
ЃН49atm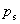 БэЪОЁЃдквЛЖЈЕФЮТЖШЯТ
БэЪОЁЃдквЛЖЈЕФЮТЖШЯТ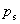 ЮЊвЛЖЈжЕЁЃ
ЮЊвЛЖЈжЕЁЃ