|
Ѓ Ѓ ЖдШЮвтЕФПЩФцбЛЗЃЌШчгвЭМжа1a2b1ЧњЯпЫљЪОЃЌПЩНќЫЦЕФПДГЩЪЧгЩаэЖрЮЂаЁПЈХЕбЛЗзщГЩЁЃвђЧњЯпФкЕФОјШШЯпЩЯЃЌЙ§ГЬдке§ЗДЗНЯђИїНјаавЛДЮЃЌаЇЙћЕжЯћЃЌЫљвдетаЉаЁбЛЗЕФзмаЇЙћЯрЕБгкЭМаЮжаЕФОтГнаЮБеКЯЧњЯпЁЃ
ЖдЦфжаШЮвЛаЁбЛЗЖМга
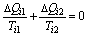
ЖдЫљгаетаЉаЁбЛЗШЁКЭЃЌОЭга
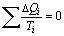
|
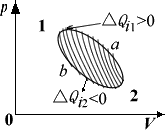
МЦЫуШЮвтПЩФцбЛЗЕФШШЮТБШ |
Ѓ Ѓ ЕБЮЂаЁПЈХЕбЛЗЪ§ФПЮоЯоЖрЪБЃЌОтГнаЮЧњЯпОЭЧїЯђдРДЕФБеКЯЧњЯпЃЌЖдШШЮТБШЧѓКЭБфГЩЛ§ЗжЃЌМД
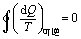
Ѓ Ѓ ЩЯЪНжаЁгБэЪОбиПЩФцбЛЗТЗОЖЛ§ЗжЁЃdQЮЊЯЕЭГгыЮТЖШЮЊ
T ЕФШШдДНгДЅЕФЮоЯоаЁЕФЙ§ГЬжаЮќЪеЕФШШСПЁЃ
Ѓ Ѓ ЖдееШЮвтПЩФцбЛЗЕФp-VЭМЃЌЩЯЪіЛ§ЗжЪНвВПЩаДГЩ
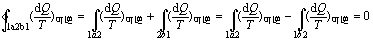
Ѓ Ѓ гЩДЫПЩЕУ
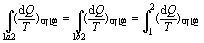
Ѓ Ѓ ЩЯЪНБэУїЯЕЭГДгзДЬЌ1ПЩвдОЮоЯоЖржжВЛЭЌЕФПЩФцЙ§ГЬЕНДязДЬЌ2ЃЌЦфШШЮТБШжЎКЭЖМЯрЕШЃЌгыЙ§ГЬЮоЙиЃЌжЛвРРЕгкЪМЁЂФЉзДЬЌЁЃвђДЫЃЌв§НјвЛИіаТЕФзДЬЌКЏЪ§SЃЌГЦжЎЮЊьиЃЈentropyЃЉЃЌВЂЖЈвхЃКЯЕЭГДгзДЬЌ1ЃЈьиЮЊS1ЃЉБфЛЏЕНзДЬЌ2ЃЈьиЮЊS2ЃЉЪБЃЌьиЕФдіСПЃЈЛђьиБфЃЉЮЊ
ЖдгкЮоЯоаЁПЩФцЙ§ГЬЃЌЦфьиБфЮЊ
ЪН(2)КЭЪН(3)ГЦЮЊПЫРЭаоЫЙьиЙЋЪНЁЃ S
ЕФЕЅЮЛШдЮЊ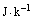
ЁЁЁЁЫЕУїЃКЂйПЫРЭаоЫЙьиSЪЧЬЌКЏЪ§ЃЌШШЮТБШЃЈ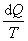 ЃЉЪЧЙ§ГЬСПЃЌ
БэЪОЯЕЭГЕФьиБфЁїS = ЃЉЪЧЙ§ГЬСПЃЌ
БэЪОЯЕЭГЕФьиБфЁїS = 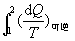 ЪЧгУПЩФцЙ§ГЬЕФШШЮТБШРДСПЖШЕФЁЃ ЪЧгУПЩФцЙ§ГЬЕФШШЮТБШРДСПЖШЕФЁЃ
Ѓ Ѓ Ѓ Ѓ Ѓ ЂкШєЯЕЭГДгзДЬЌ1ЕНзДЬЌ2ЕФЙ§ГЬЪЧВЛПЩФцЕФЃЌПЩвджЄУї ЁїS >
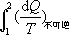 ЃЌМДЦфьиБфВЛФмгУ ЃЌМДЦфьиБфВЛФмгУ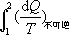 МЦЫуЁЃвђЮЊьиЪЧЬЌКЏЪ§гыЙ§ГЬЮоЙиЃЌЫљвдПЩШЮбЁвЛИіСЌНгзДЬЌ1КЭзДЬЌ2ЕФПЩФцЙ§ГЬДњЬцВЛПЩФцЙ§ГЬНјааМЦЫуЃК
МЦЫуЁЃвђЮЊьиЪЧЬЌКЏЪ§гыЙ§ГЬЮоЙиЃЌЫљвдПЩШЮбЁвЛИіСЌНгзДЬЌ1КЭзДЬЌ2ЕФПЩФцЙ§ГЬДњЬцВЛПЩФцЙ§ГЬНјааМЦЫуЃК
Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ Ѓ ЁїS=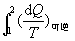
Ѓ Ѓ Ѓ Ѓ Ѓ ЂлПЫРЭаоЫЙьигыВЃЖњзШТќьидкБОжЪЩЯЪЧЕШМлЕФЁЃ
ЁЁЁЁвдЦјЬхОјШШздгЩХђеЭЮЊР§ЃЌЧАУцЮвУЧвбОИљОнВЃЖњзШТќьиЙЋЪНЃЌМЦЫуГіСЫЦјЬхОјШШздгЩХђеЭЙ§ГЬЕФьиБфЮЊ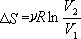 ЃЌЯждкгУПЫРЭаоЫЙьиЙЋЪНжиаТМЦЫуРэЯыЦјЬхдкОјШШздгЩХђеЭЙ§ГЬжаЕФьиБфЁЃ ЃЌЯждкгУПЫРЭаоЫЙьиЙЋЪНжиаТМЦЫуРэЯыЦјЬхдкОјШШздгЩХђеЭЙ§ГЬжаЕФьиБфЁЃ
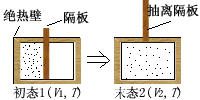
ЦјЬхОјШШздгЩХђеЭЙ§ГЬьиЕФМЦЫу
|
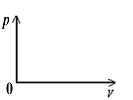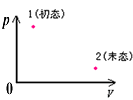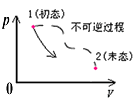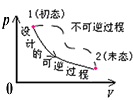
ПЩФцЕШЮТХђеЭЙ§ГЬЃЈЪЕЯпЃЉ
КЭздгЩХђеЭЙ§ГЬЃЈащЯпЃЉ |
Ѓ Ѓ вђЦјЬхОјШШздгЩХђеЭЪБЃЌФЉЬЌ2ЕФЮТЖШTКЭГѕЬЌ1ЕФЮТЖШЯрЭЌЁЃЫљвдПЩбЁдёвЛИіПЩФцЕШЮТХђеЭЙ§ГЬСЌНгзДЬЌ1КЭзДЬЌ2ЃЌЃЈМћЩЯгвЭМЃЉРДМЦЫуЁїSЃЎ
Ѓ Ѓ гЩШШСІбЇЕквЛЖЈТЩЃЌдкЕШЮТЙ§ГЬжаЃЌdE= 0ЃЌdQ=dA=pdVЃЌЫљвд
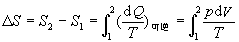
НЋРэЯыЦјЬхзДЬЌЗНГЬ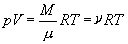 ДњШыЩЯЪНЃЌПЩЕУ ДњШыЩЯЪНЃЌПЩЕУ
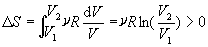
Ѓ Ѓ ДЫНсЙћгыЧАУцгЩВЃЖњзШТќьиЙЋЪНЭЦЕМЕФьиБфЙЋЪНЭъШЋЯрЭЌЁЃ
4ЁЂПЫРЭаоЫЙьиВЛЕШЪН
Ѓ Ѓ ЖдгкВЛПЩФцПЈХЕбЛЗЃЌгЩПЈХЕЖЈРэ 2
ПЩжЊ
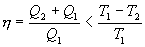
ЪНжа 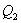 < 0ЁЃгЩДЫПЩЕУШШЮТБШжЎКЭЮЊ
< 0ЁЃгЩДЫПЩЕУШШЮТБШжЎКЭЮЊ
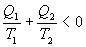
|
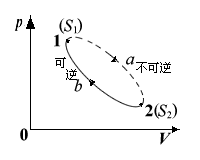
МЦЫуВЛПЩФцбЛЗЕФШШЮТБШ |
|
