 作业选解
作业选解
03-08-05-07 空气是一种混合气体,其中几种主要成分的体积百分比是:氮(N2)
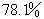 ,氧(O2)
,氧(O2) 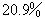 ,氩(Ar)
,氩(Ar) 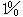 ,它们的分子量分别是28.0、32.0、39.9,求在标准状态下空气中这三种主要组分的分压强、密度,并由此求空气的密度和平均摩尔质量。
,它们的分子量分别是28.0、32.0、39.9,求在标准状态下空气中这三种主要组分的分压强、密度,并由此求空气的密度和平均摩尔质量。
解: 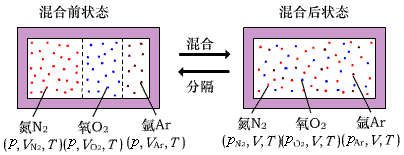
如图所示,设在 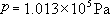 和
和 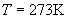 的标准状态下,空气的体积为V 。则三种组分的体积分别为
的标准状态下,空气的体积为V 。则三种组分的体积分别为
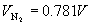 ,
, 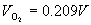 ,
, 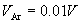
由于气体混合过程中温度T 保持不变,则当这三种气体混合成标准状态的空气后,其状态分别从 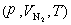 、
、
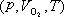 、
、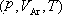 变为
变为 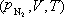 、
、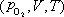 、
、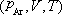 。
。
由理想气体状态方程 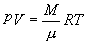 或
或 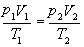 ,可得
,可得
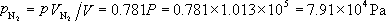
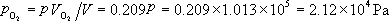
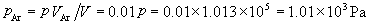
各组分的密度分别为
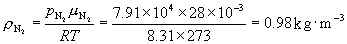
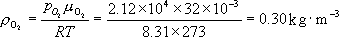
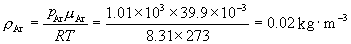
于是得空气的密度为: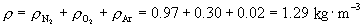
混合气体的质量 M 为其中各组分的质量之和,即 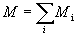 ,定义混合气体的平均摩尔质量 μ 如下式
,定义混合气体的平均摩尔质量 μ 如下式
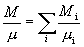 或
或 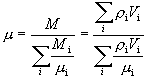
代入有关数据后,得 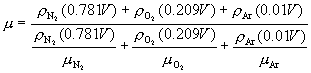
= 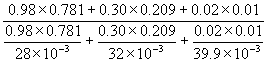
= 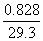 =
= 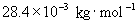 (注)
(注)